Los probióticos son microorganismos vivos que, administrados en cantidades adecuadas, confieren beneficios a la salud del huésped, según la definición consenso de la ISAPP. Las cepas más estudiadas pertenecen a los géneros Lactobacillus, Bifidobacterium y a la levadura Saccharomyces boulardii. Actúan modulando la microbiota intestinal, reforzando la barrera epitelial y regulando la respuesta inmune. Las dosis eficaces suelen situarse entre 1.000 y 50.000 millones de UFC al día, con resultados cepa-específicos en diarrea asociada a antibióticos, síndrome de intestino irritable e inmunidad.
- Definición ISAPP 2014: microorganismos vivos que, en cantidades adecuadas, confieren un beneficio a la salud del huésped.
- Los efectos son cepa-específicos: no todas las cepas de Lactobacillus o Bifidobacterium hacen lo mismo ni sirven para lo mismo.
- Dosis habitual: entre 1.000 y 50.000 millones de UFC al día; los efectos clínicos requieren el uso continuado durante 4 a 12 semanas.
- Saccharomyces boulardii y Lactobacillus rhamnosus GG reducen el riesgo de diarrea asociada a antibióticos en niños y adultos según revisiones Cochrane.
¿Qué es un probiótico?
Un probiótico es un microorganismo vivo que, administrado en cantidades adecuadas, confiere un beneficio a la salud del huésped. Esta definición fue adoptada oficialmente por la International Scientific Association for Probiotics and Prebiotics (ISAPP) en 2014 y sigue siendo la referencia científica actual (Hill et al., 2014). El término engloba principalmente a bacterias de los géneros Lactobacillus y Bifidobacterium, y a levaduras como Saccharomyces boulardii, cuyas cepas específicas cuentan con estudios clínicos que respaldan efectos concretos sobre la microbiota intestinal, la digestión y el sistema inmune.
No cualquier microorganismo es un probiótico: para recibir esa denominación debe estar vivo al momento del consumo, identificado hasta nivel de cepa (no solo género y especie), haber demostrado seguridad y beneficios en ensayos clínicos bien diseñados, y administrarse en una dosis consistente con la evidencia. Los probióticos se diferencian así de los fermentos alimentarios tradicionales, de los postbióticos (metabolitos derivados) y de los prebióticos, que son las fibras fermentables que alimentan a estas bacterias.
¿Para qué sirven los probióticos?
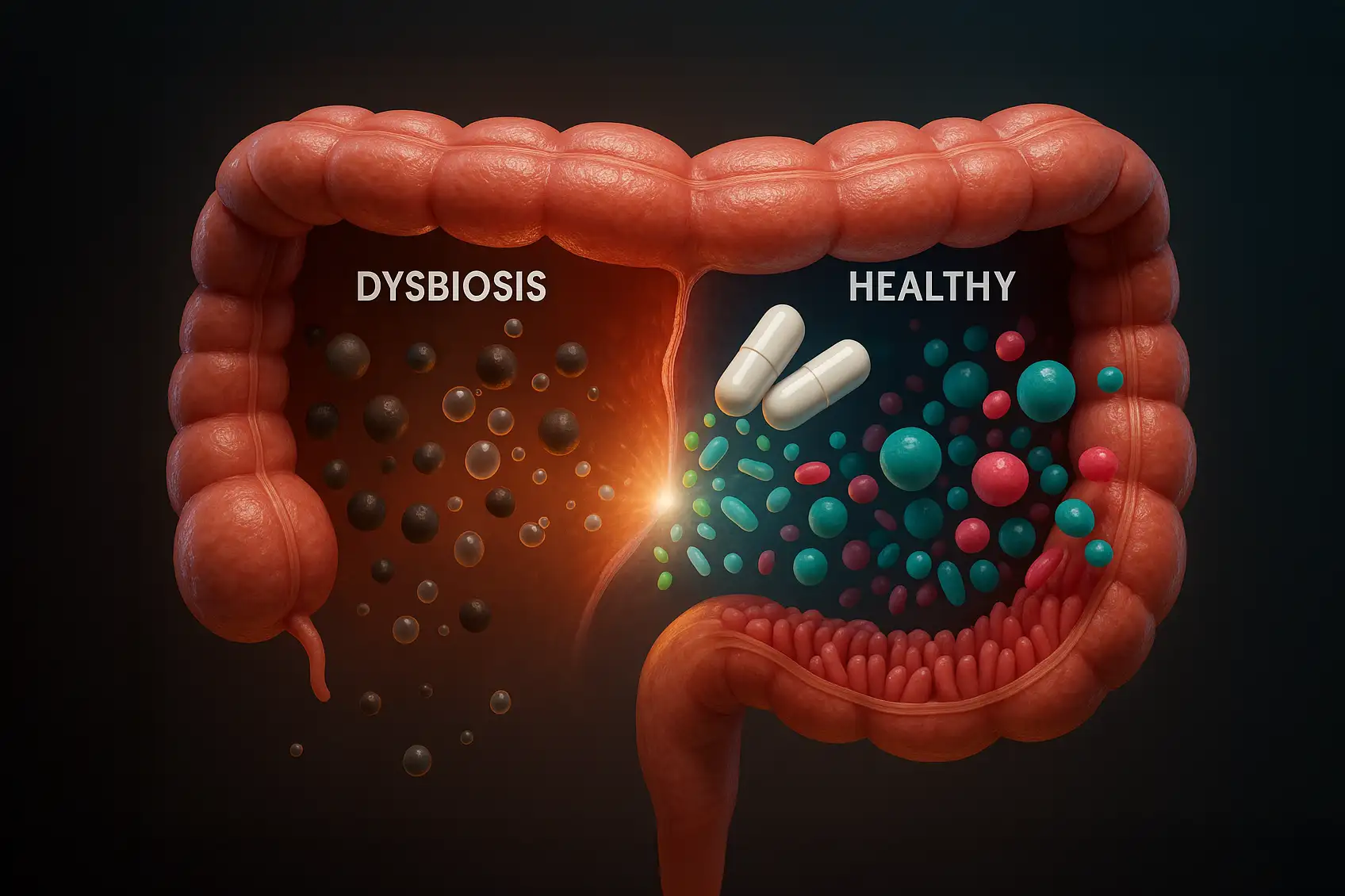
Los probióticos actúan principalmente sobre tres frentes: el equilibrio de la microbiota intestinal, la barrera epitelial del intestino y la modulación del sistema inmune. Su utilidad clínica más consolidada se centra en la prevención de la diarrea asociada a antibióticos, el manejo de síntomas del síndrome de intestino irritable (SII), el apoyo en casos de diarrea aguda infantil y la reducción de infecciones respiratorias leves en ciertas poblaciones (Markowiak & Śliżewska, 2017).
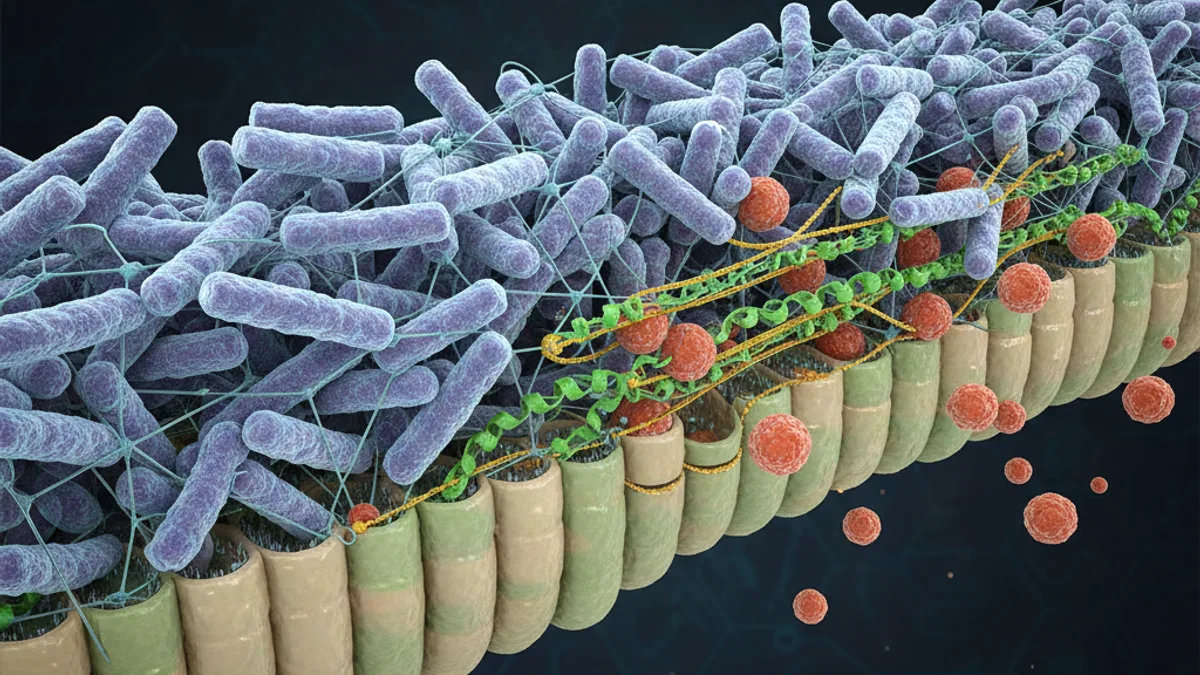
Los mecanismos biológicos que explican estos efectos incluyen la competencia por nutrientes y sitios de adhesión frente a patógenos, la producción de ácidos orgánicos y bacteriocinas con actividad antimicrobiana, el refuerzo de las uniones estrechas entre enterocitos, la estimulación de la producción de mucina y la regulación de citoquinas pro- y antiinflamatorias. Es importante entender que los beneficios son cepa-específicos: un estudio positivo con Lactobacillus rhamnosus GG no extrapola automáticamente a otras cepas, ni siquiera dentro de la misma especie.
Cepas principales de probióticos
El universo probiótico comercial se concentra en pocas familias microbianas con respaldo clínico sólido. Conocer a quién pertenece cada cepa ayuda a elegir una fórmula con criterio en lugar de por marketing.
Género Lactobacillus
El género Lactobacillus (hoy reclasificado taxonómicamente en varios géneros, pero comercialmente aún agrupado bajo ese nombre) incluye bacterias ácido lácticas que habitan el tracto digestivo, la boca y el tracto urogenital. Entre las cepas más estudiadas destacan Lactobacillus acidophilus NCFM, Lactobacillus reuteri DSM 17938 y Lactobacillus rhamnosus GG, respaldada por cientos de ensayos en diarrea infantil y diarrea del viajero.
Género Bifidobacterium
Los bifidobacterias son dominantes en la microbiota del lactante amamantado y mantienen un papel relevante en el colon adulto. Cepas como Bifidobacterium bifidum, Bifidobacterium longum y Bifidobacterium lactis BB-12 han demostrado beneficios sobre la regularidad intestinal, la reducción de la distensión abdominal y el soporte inmune, particularmente en lactantes y adultos mayores (Sjælland et al., 2025).
Saccharomyces boulardii
Saccharomyces boulardii CNCM I-745 es una levadura —no una bacteria— dentro del género Saccharomyces. Su característica distintiva es que resiste la toma concomitante de antibióticos, ya que los antimicrobianos no la afectan. Ensayos clínicos y metanálisis la posicionan como una de las intervenciones más sólidas para la prevención de la diarrea asociada a antibióticos, la diarrea aguda infecciosa en pediatría y como adyuvante en la erradicación de Helicobacter pylori (Li & McFarland, 2026; Ma et al., 2025).
Otras cepas relevantes
- Bacillus coagulans: bacteria formadora de esporas, estable a temperatura ambiente, con evidencia en molestias digestivas funcionales.
- Lactococcus lactis: utilizada en industria láctea y estudiada como moduladora de células dendríticas plasmocitoides e inmunidad respiratoria.
- Streptococcus thermophilus: presente en yogures, contribuye al alivio de la intolerancia a la lactosa.
Probióticos y salud digestiva
La aplicación con mayor volumen de evidencia es la salud digestiva. En el síndrome de intestino irritable (SII), revisiones sistemáticas recientes muestran que ciertas combinaciones multicepa pueden mejorar el dolor abdominal, la hinchazón y la calidad de vida, con mayor beneficio en subtipos específicos del SII cuando la cepa se elige según el fenotipo dominante (Almalki et al., 2025; Anwar et al., 2026).
En la diarrea aguda infantil, S. boulardii y L. rhamnosus GG reducen la duración del cuadro en aproximadamente 24 a 30 horas frente a placebo. También se ha descrito mejoría en trastornos como el estreñimiento funcional, el sobrecrecimiento bacteriano del intestino delgado (SIBO) y los síntomas digestivos asociados al estrés (Noorwali et al., 2025). En todos los casos, la evidencia exige seleccionar la cepa adecuada para la indicación concreta, no un «probiótico genérico».
Probióticos e inmunidad
Aproximadamente el 70 % del tejido inmune del organismo se encuentra en el intestino, en el llamado GALT (gut-associated lymphoid tissue). Los probióticos interactúan con las células dendríticas, los macrófagos y los linfocitos T y B de la mucosa, modulando la producción de IgA secretora, interferones y citoquinas reguladoras. Metanálisis muestran reducciones modestas pero consistentes en la incidencia y duración de infecciones respiratorias superiores en niños y adultos que consumen determinadas cepas durante al menos 8 a 12 semanas (Kato et al., 2025).
También se han descrito efectos favorables en el eje intestino-cerebro, con ensayos que reportan disminución del estrés percibido y mejoría del estado de ánimo en adultos jóvenes sanos tras suplementación multicepa. La magnitud del efecto es variable y depende de la cepa, la dosis, la duración y las características del huésped.
Probióticos y antibióticos: cuándo tomarlos
La diarrea asociada a antibióticos (DAA) afecta hasta al 30 % de las personas que reciben un tratamiento antibiótico, y una fracción relevante evoluciona hacia diarrea por Clostridioides difficile. La evidencia más sólida apoya el uso concomitante de Saccharomyces boulardii y de Lactobacillus rhamnosus GG, que reducen significativamente el riesgo de DAA y de infección por C. difficile en adultos y niños (Esmaeilinezhad et al., 2025; Wei et al., 2026).
La recomendación práctica es iniciar el probiótico el mismo día que el antibiótico y mantenerlo durante al menos una o dos semanas después de finalizar el ciclo antimicrobiano. Para las cepas bacterianas sensibles, conviene espaciar la toma unas 2 a 3 horas respecto al antibiótico; S. boulardii, al ser una levadura, puede tomarse junto con el fármaco sin perder viabilidad.
UFC: unidades formadoras de colonias
La potencia de un probiótico se expresa en unidades formadoras de colonias (UFC o CFU por sus siglas en inglés), que representan la cantidad de microorganismos viables capaces de reproducirse bajo condiciones controladas. Los productos comerciales suelen declarar entre 1.000 millones (1 × 10⁹) y 100.000 millones (1 × 10¹¹) de UFC por dosis diaria.
Una mayor cantidad de UFC no implica automáticamente mayor eficacia: lo determinante es que la dosis coincida con la utilizada en los estudios que demostraron el efecto para esa cepa específica. Un fabricante de calidad declara las UFC garantizadas hasta el final de la vida útil del producto, identifica las cepas con nombre completo y código (por ejemplo, L. rhamnosus GG o B. lactis BB-12) y protege a las bacterias de la humedad, el calor y la acidez gástrica mediante tecnologías como la microencapsulación o las cápsulas entéricas.
Fuentes naturales de probióticos
Muchas culturas incorporan alimentos fermentados como vehículo tradicional de probióticos, aunque con una composición y concentración menos estandarizadas que las de los suplementos clínicos.
- Kéfir de leche y de agua: combina bacterias ácido lácticas y levaduras en una matriz fermentada rica en cepas.
- Yogur natural no pasteurizado tras la fermentación: aporta Streptococcus thermophilus y Lactobacillus delbrueckii subsp. bulgaricus.
- Chucrut y kimchi: vegetales fermentados con Lactobacillus plantarum y otras especies.
- Kombucha: té fermentado con un consorcio de bacterias y levaduras (SCOBY).
- Miso, tempeh y natto: derivados de la soja fermentada tradicionales en la cocina asiática.
Estos alimentos aportan además ácidos orgánicos, péptidos bioactivos y, en combinación con fibras como la inulina o la fibra dietética, actúan como base de una dieta simbiótica. Para indicaciones clínicas concretas, sin embargo, las dosis y cepas controladas de los suplementos probióticos ofrecen una evidencia más precisa.
Dosis y duración recomendadas
La dosis efectiva depende de la cepa y la indicación. Los rangos habituales son:
- Mantenimiento digestivo general: 1.000 a 10.000 millones de UFC al día, de forma continuada.
- Diarrea asociada a antibióticos: S. boulardii 250-500 mg dos veces al día o L. rhamnosus GG 10.000 millones de UFC al día, durante el tratamiento y 1-2 semanas posteriores.
- Síndrome de intestino irritable: fórmulas multicepa entre 5.000 y 50.000 millones de UFC al día durante al menos 4 a 8 semanas.
- Soporte inmune: 1.000 a 10.000 millones de UFC al día durante al menos 8 a 12 semanas antes de esperar efectos.
La toma suele recomendarse en ayunas o antes de las comidas, con agua a temperatura ambiente para no comprometer la viabilidad de las cepas. En Suplenet curamos marcas como Thorne, Garden of Life, Metagenics, Nordic Naturals y NOW Foods, que declaran cepas, dosis y UFC garantizadas con trazabilidad, en nuestra categoría de salud digestiva.
Efectos secundarios y contraindicaciones
Los probióticos tienen un perfil de seguridad muy favorable en población general sana. Los efectos adversos más frecuentes son leves: distensión abdominal, flatulencia o deposiciones más blandas durante los primeros días, que tienden a resolverse por sí solos al adaptarse la microbiota. En algunas personas sensibles pueden aparecer brotes transitorios de hinchazón cuando se combinan con prebióticos muy fermentables como la inulina.
Las principales precauciones se concentran en poblaciones específicas: pacientes inmunocomprometidos (quimioterapia, trasplantados, VIH avanzado), recién nacidos prematuros, personas con catéteres venosos centrales o válvulas cardíacas protésicas y pacientes críticos en unidades de cuidados intensivos. En estos grupos se han descrito casos raros pero documentados de bacteriemia y fungemia por cepas probióticas, por lo que cualquier uso debe valorarse con el médico tratante.