Las cepas L. rhamnosus GR-1 y L. reuteri RC-14 por vía oral migran del intestino a la vagina y reducen recurrencias de VB (88% vs 40%) y candidiasis (7% vs 35%). La colonización efectiva requiere ≥10⁹ UFC/día durante mínimo 8-12 semanas como adyuvante al tratamiento estándar.
- L. rhamnosus GR-1 y L. reuteri RC-14 son las cepas con mayor evidencia para salud vaginal oral
- Los probióticos orales migran desde el intestino a la vagina por la ruta perineal confirmada molecularmente
- La combinación antibiótico + probiótico duplica la tasa de curación de vaginosis bacteriana
- Los probióticos son adyuvantes — no reemplazan el tratamiento antibiótico o antifúngico de primera línea
- La identificación de cepa específica (no solo especie) es determinante para la eficacia clínica
La microbiota vaginal es un ecosistema extraordinariamente dinámico cuyo equilibrio depende, en gran medida, de la predominancia de especies de Lactobacillus. Cuando esa predominancia se pierde — por antibióticos, estrés, fluctuaciones hormonales o disbiosis intestinal — aparecen dos de las infecciones vaginales más prevalentes en el mundo: la vaginosis bacteriana (VB) y la candidiasis vulvovaginal (CVV).
Lo que resulta fascinante desde el punto de vista microbiológico es que la restauración de la flora vaginal no requiere necesariamente una intervención local. La administración oral de cepas probióticas específicas ha demostrado capacidad de migrar desde el tracto gastrointestinal hasta la mucosa vaginal, colonizarla y restablecer el equilibrio microbiano1. Este artículo examina la evidencia detrás de esta ruta oral-vaginal y las cepas con mayor respaldo científico.
La microbiota vaginal saludable: dominancia de Lactobacillus
En mujeres en edad reproductiva, la microbiota vaginal saludable está dominada por una o varias especies de Lactobacillus: L. crispatus, L. iners, L. jensenii y L. gasseri son las más frecuentes. Estas bacterias cumplen funciones protectoras esenciales:
- Producción de ácido láctico: mantiene el pH vaginal entre 3.8 y 4.5, creando un ambiente hostil para patógenos.
- Producción de peróxido de hidrógeno (H₂O₂): L. crispatus es particularmente eficiente en esto, y el H₂O₂ tiene actividad bactericida directa contra Gardnerella vaginalis y otras bacterias asociadas a VB2.
- Producción de bacteriocinas: péptidos antimicrobianos que inhiben el crecimiento de competidores.
- Competencia por adhesión: los lactobacilos ocupan los receptores epiteliales, impidiendo la adhesión de patógenos.
Cuando esta barrera se rompe, Gardnerella vaginalis, Atopobium vaginae, Prevotella spp. y otros anaerobios proliferan (VB), o Candida albicans y especies no-albicans aprovechan la oportunidad para sobrecrecer (CVV).
La ruta oral-vaginal: cómo llegan los probióticos del intestino a la vagina
La conexión intestino-vagina es uno de los hallazgos más relevantes en microbiología clínica reciente. Estudios de secuenciación genómica han confirmado que las mismas cepas de Lactobacillus presentes en el intestino pueden identificarse posteriormente en la mucosa vaginal tras administración oral3.
El mecanismo propuesto implica la migración perineal: los lactobacilos ingeridos oralmente colonizan el tracto gastrointestinal, son excretados, y desde la región perianal migran hacia el introito vaginal y ascienden por la mucosa. Este proceso no es teórico — ha sido confirmado mediante ribotipado molecular que permite rastrear cepas específicas desde la cápsula hasta la vagina4.

La ventaja de la ruta oral sobre la vaginal es evidente: mejor adherencia terapéutica, ausencia de incomodidad local, y la capacidad de tratar simultáneamente la disbiosis intestinal que frecuentemente subyace a la disbiosis vaginal.
Las cepas con mayor evidencia: L. rhamnosus GR-1 y L. reuteri RC-14
No todos los probióticos son iguales, y en salud vaginal esta máxima es especialmente crítica. Las dos cepas con mayor cantidad de evidencia clínica son Lactobacillus rhamnosus GR-1 y Lactobacillus reuteri RC-14 (anteriormente clasificada como L. fermentum RC-14).
El Dr. Gregor Reid y su equipo en la Universidad de Western Ontario han sido los principales investigadores de esta combinación durante más de dos décadas. Sus hallazgos clave incluyen:
Vaginosis bacteriana
Un ensayo controlado aleatorizado en 125 mujeres con VB comparó el tratamiento estándar con metronidazol solo versus metronidazol + L. rhamnosus GR-1/L. reuteri RC-14 oral (10⁹ UFC, dos veces al día durante 30 días). El grupo combinado mostró una tasa de curación del 88% versus 40% en el grupo de metronidazol solo a las 30 días post-tratamiento5.
Otro estudio en mujeres con VB recurrente (≥3 episodios/año) demostró que la administración oral diaria de estas cepas durante 60 días redujo las recurrencias en un 73% durante los 6 meses de seguimiento6.
Candidiasis vulvovaginal
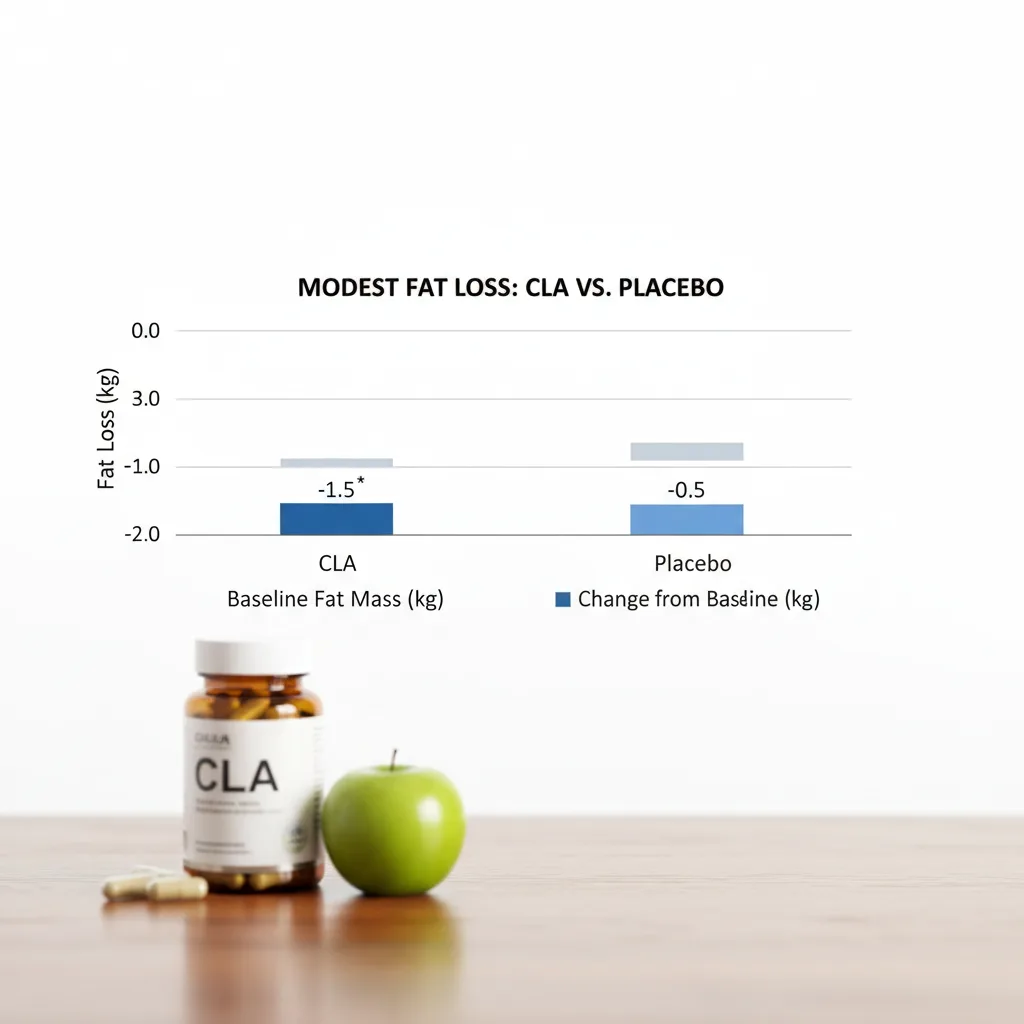
En candidiasis recurrente, la evidencia es igualmente promisoria. Un ensayo en 55 mujeres con CVV recurrente (≥4 episodios/año) mostró que la suplementación oral con GR-1/RC-14 como adyuvante al tratamiento antifúngico estándar (fluconazol) redujo la tasa de recurrencia a los 6 meses del 35% al 7%7.
El mecanismo propuesto es dual: restauración directa de la barrera de lactobacilos vaginales + modulación de la respuesta inmune mucosa (aumento de IgA secretora y citocinas antiinflamatorias en la mucosa vaginal).
Otras cepas con evidencia emergente
Además de GR-1 y RC-14, varias cepas están acumulando evidencia clínica:
| Cepa | Indicación principal | Nivel de evidencia | Mecanismo destacado |
|---|---|---|---|
| L. crispatus CTV-05 (Lactin-V) | Prevención de VB recurrente | Fase III (RCT publicado en NEJM) | Productor potente de H₂O₂ y ácido láctico |
| L. acidophilus LA-5 | VB y CVV como adyuvante | Múltiples RCTs | Adhesión epitelial competitiva |
| L. plantarum P17630 | CVV recurrente | RCTs (vía vaginal) | Inhibición de formación de hifas de Candida |
| L. rhamnosus BMX 54 (Normogin®) | VB recurrente | RCTs | Restauración del pH vaginal |
Es importante señalar que L. crispatus CTV-05 (Lactin-V) fue evaluado en un ensayo fase III publicado en el New England Journal of Medicine en 2020, donde demostró reducir la recurrencia de VB en un 30% comparado con placebo tras tratamiento con metronidazol. Sin embargo, este producto se administra por vía vaginal, no oral8.
Protocolos prácticos: dosis, duración y timing
Basándose en la evidencia disponible, los protocolos con mayor respaldo son:
Para prevención de VB recurrente
- Cepas: L. rhamnosus GR-1 + L. reuteri RC-14
- Dosis: ≥10⁹ UFC totales por día (idealmente 2×10⁹ UFC)
- Duración mínima: 8-12 semanas para colonización efectiva
- Mantenimiento: ciclos de 30 días on / 30 días off, evaluando recurrencia
- Timing: iniciar simultáneamente con el tratamiento antibiótico (separar la toma por al menos 2 horas)
Para prevención de CVV recurrente
- Cepas: L. rhamnosus GR-1 + L. reuteri RC-14 (o L. acidophilus LA-5 como alternativa)
- Dosis: ≥10⁹ UFC totales por día
- Duración: mínimo 12 semanas como adyuvante post-antifúngico
- Consideración: en pacientes con candidiasis recurrente, abordar simultáneamente la disbiosis intestinal (reducir azúcares refinados, considerar fibra prebiótica)

Factores que potencian la eficacia de los probióticos vaginales
La suplementación probiótica no actúa en un vacío. Su eficacia se modula significativamente por factores del huésped:
- Fibra prebiótica: los fructooligosacáridos (FOS) y la inulina alimentan selectivamente a los lactobacilos tanto intestinales como vaginales. Una dieta rica en fibra soluble crea las condiciones para que los probióticos proliferen tras la colonización.
- Estrógenos: los estrógenos estimulan la producción de glucógeno en el epitelio vaginal, que es el sustrato principal para la fermentación láctica por Lactobacillus. En mujeres perimenopáusicas o con hipoestrogenismo, la eficacia de los probióticos puede ser menor sin estrogenoterapia local complementaria.
- Antibióticos sistémicos: cada curso de antibióticos de amplio espectro depleta tanto la microbiota intestinal como la vaginal. Los probióticos deben reiniciarse tras cada tratamiento antibiótico, separando la toma por al menos 2 horas.
- Higiene íntima: los jabones con pH alcalino, las duchas vaginales y los productos perfumados destruyen la barrera de lactobacilos. La evidencia apoya el uso exclusivo de agua o limpiadores con pH 3.8-4.5.
Cuándo los probióticos orales no son suficientes
Es fundamental mantener expectativas realistas. Los probióticos orales son una estrategia adyuvante y preventiva, no un tratamiento de primera línea para infecciones activas:
- VB sintomática activa: requiere tratamiento antibiótico (metronidazol o clindamicina) seguido de probióticos para prevenir recurrencia.
- CVV activa: requiere tratamiento antifúngico (fluconazol oral o azoles tópicos) seguido de probióticos como mantenimiento.
- Infecciones por Candida no-albicans: especies como C. glabrata o C. krusei son intrínsecamente resistentes a los azoles y pueden requerir esquemas antifúngicos especializados. Los probióticos son un complemento, no una solución independiente.
- VB asociada a biofilm: Gardnerella vaginalis forma biofilms adherentes que son particularmente resistentes tanto a antibióticos como a la competencia por lactobacilos. Protocolos disruption-then-replace (disrupción del biofilm + recolonización probiótica) están en investigación.
Nomenclatura y selección de productos: lo que debes verificar
La precisión en la nomenclatura de cepas es determinante. Un producto que lista simplemente "Lactobacillus rhamnosus" sin especificar la cepa GR-1 no tiene la misma evidencia. Las características probióticas son cepa-específicas, no especie-específicas9.
Al evaluar un producto probiótico para salud vaginal, verifica:
- Identificación de cepa completa (género + especie + designación de cepa): ej. Lactobacillus rhamnosus GR-1, no solo "L. rhamnosus"
- UFC garantizadas al vencimiento, no al momento de fabricación (la diferencia puede ser de varios logaritmos)
- Estudios clínicos propios con la formulación específica del producto
- Condiciones de almacenamiento: algunas cepas requieren refrigeración para mantener viabilidad
Perspectiva del microbioma: más allá del tratamiento agudo
La tendencia en microbiología clínica se está moviendo hacia la medicina de microbioma personalizada. Tests de secuenciación vaginal (como el Evvy o el Juno Bio) permiten identificar la composición exacta de la microbiota de cada paciente y diseñar intervenciones probióticas dirigidas.
Lo que parece claro es que el futuro del manejo de las infecciones vaginales recurrentes no está en ciclos repetidos de antibióticos y antifúngicos que perpetúan la disbiosis, sino en la restauración ecológica del microbioma. Los probióticos orales, con las cepas correctas a las dosis adecuadas, son una herramienta valiosa en esa dirección10.
El tratamiento de la vaginosis y la candidiasis recurrentes no termina cuando los síntomas desaparecen. Termina cuando la microbiota vaginal recupera su equilibrio y puede defenderse sola.